肿瘤来源的外泌体(exosomes)在肿瘤微环境的胞间通讯中发挥着特殊作用,它们在体液中含量稳定且能够灵敏地反映出肿瘤的实际状态,被认为是“液体活检”技术中一种极具潜力的肿瘤标志物。外泌体研究中面临的首要困难是如何从复杂的生物样品中分离出这些微小囊泡,超速离心法是外泌体浓缩的经典方法,但步骤冗杂、仪器昂贵,且回收率较低。对外泌体进行定量的标准方法,例如ELISA和western blot,在需要较大样品量的同时,其灵敏度较低。此外,分步对外泌体进行处理和分析的过程不仅耗时耗力,样品也极易受到外界的污染。
近日,华东理工大学的叶邦策教授团队报道了一种集分离、富集和检测为一体的肝癌相关外泌体分析平台(ExoPCD-chip)。该微流控芯片由一个Y型微柱阵列组成的捕获区域和级联的ITO电极组成。预先修饰有Tim4蛋白的磁珠可以特异结合外泌体表面暴露出的磷酯酰丝氨酸,而芯片中的PDMS微柱则进一步增强磁珠对外泌体的捕获效率。富集到的外泌体随后被磁力固定在ITO电极的表面,通过一条包含CD63识别序列和模拟DNA酶序列的核酸适配体来实现电化学信号转换的过程,在快速、高特异性外泌体识别的基础上实现了高灵敏的电化学传感分析。
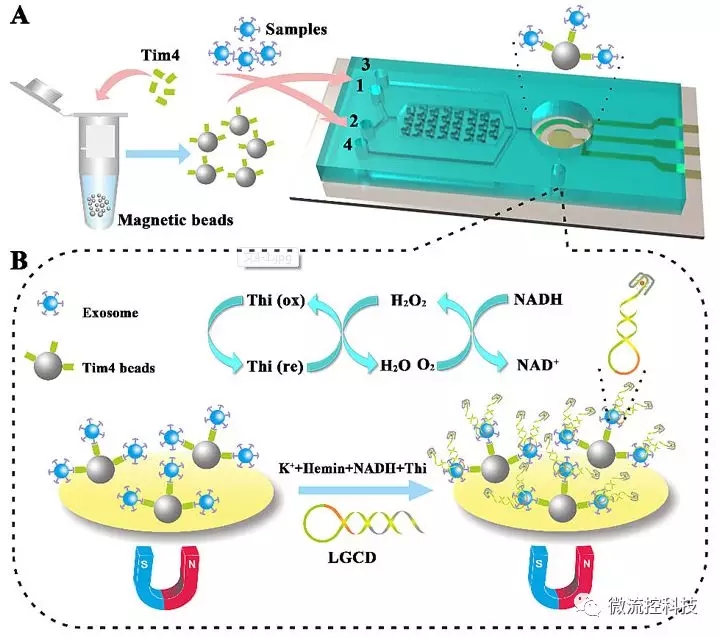
图1.(A)ExoPCD-chip示意图;(B)ITO表面电传感示意图
该ExoPCD-chip仅需30 μL样品,在4小时内即可完成整个分离富集和检测的全过程,其检出限低于目前绝大多数文献中报道的结果。更为重要的是,对血清样品的分析结果证明,该芯片能够有效区分肝癌病人和健康人,具有临床检测和癌症诊断的潜力。
相关研究成果近期发表在Analytical Chemistry 上,文章的第一作者为华东理工大学的讲师徐慧颖和硕士生廖翀。
论文信息:Huiying Xu, Chong Liao, Peng Zuo, Ziwen Liu and Bang-Ce Ye, Magnetic-Based Microfluidic Device for On-Chip Isolation and Detection of Tumor-Derived Exosomes, Anal. Chem., 2018, 90, 13451, DOI: 10.1021/acs.analchem.8b03272.
(文章来源:X-MOL 科学网科学网转载仅供参考学习及传递有用信息,版权归原作者所有,如侵犯权益,请联系删除)


