心血管疾病往往是由微小血管的结构和功能的病变积累而引起的。一份2003年的“国家健康与营养调查”的报告说:患有高血压人数的比例正在上升。因此,模拟动脉生物反应的微流控平台具有极其重要的意义:不仅能够在整个药物开发试验中能更真实地模拟器官屏障,而且还可以全面了解小动脉病理变化的潜在机制,对于制定更好的心血管疾病治疗策略十分有益。来自多伦多大学的Axel Gunther认为,这种基于MEMS的设备可能有助于在临床环境(精细医学)中评估患者的微血管所处的状态。
用于分离检查的电阻血管(直径在30μm和300μm之间的微动脉和小动脉)固有特性的常规方法包括压力肌成像技术。目前这种方法无法扩展增加其他功能,而且对技术人员的技能要求颇高,因此,无法大面积推广开来。然而,基于微流控芯片技术的动脉体外模拟可以克服这几个限制,能够进行功能扩展、制造成本低、且能有够实现自动化的可能性。
Example 例子:
已经开发了一种基于微流控技术的器官芯片装置作为实验研究平台,可以将脆性血管固定在上面,进而能够研究阻力动脉畸形的决定因素。动脉微环境的特点复杂,是由周围温度,透壁压、腔内压和体外药物浓度构成。来自微环境中的多个机械或化学输入刺激分别引起平滑肌细胞(SMC)和内皮细胞(EC)上在血管的外壁和腔壁进行排列。内皮细胞负责释放血管收缩和血管舒张因子,从而改变了血管收缩节律。血管收缩节律定义为血管相对于其最大直径的收缩程度。
目前的导致疾病发生的概念认为,此微环境的细微变化对动脉节律有明显的影响,可在很大程度上改变外周血管阻力。设计此结构的工程师认为,这一装置具体的优势在于其模拟和控制微环境中异质时空影响因素的能力,通过向外壁的两个通道之一传递苯肾上腺素,使得而面向药物的一侧比药物相对侧更容易收缩。
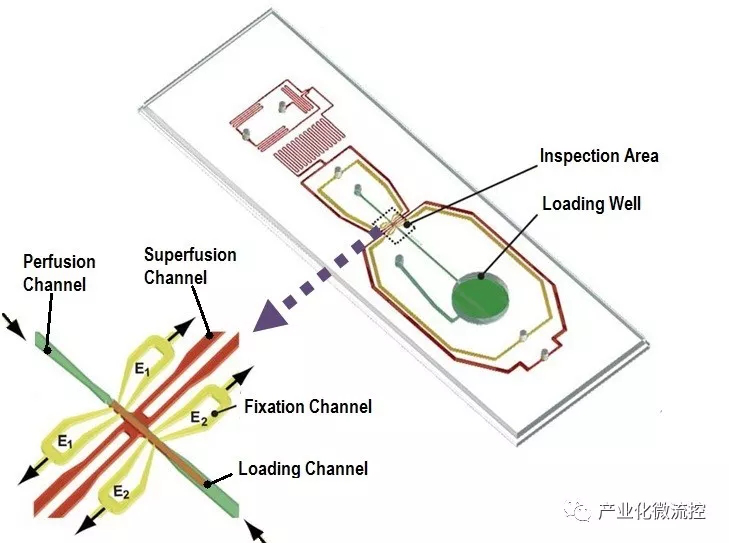
图1 芯片动脉及检测区域的技术细节描述:绿色微通道用于装载动脉段,并通过灌注液体将营养物质输送到腔壁; 黄色的固定通道通过在每个端部施加次大气压力来用于调整检查区域中器官的位置; 红色是灌注通道,用于将营养物质输送到动脉的外膜壁。
所设计的基于微流控芯片的动脉可实现样品的可逆植入。该装置包含微通道网络,动脉加载区域和单独的动脉检查区域。用于装载动脉的微通道,且当装载腔室被密封后,可作为灌注通道,以实现在生物组织中将动脉血的营养传递到毛细血管床。另一对微通道用于固定动脉段的两端。最后一对微通道用于提供流量率的融合,以便通过朝腹腔壁上传送稳定的维持培养基,用于保持器官的生理和代谢活动。
再通过把热电加热器和热敏电阻连接到芯片,能够保持并检查动脉区域的生理温度。
加载和固定组织样本到检测区域的方法有助于了解此微流控芯片是如何确认整个器官功能的。将组织片段浸入到装载孔后,通过注射器在装载通道的远端释放恒定流速的缓冲溶液驱动装载过程。这样的结构和外界装置可以确保将动脉运送到其特定的位置。此过程依赖于通过封闭的固定和灌注输入/输出线完成的。当注射泵停止之后,可通过其中一个固定通道施加低于大气压的压力。然后在密封装载孔封闭之后,第二固定通道受到低于大气压的压力。在检测区域建立对称的动脉组,而且该段感受到跨壁压力。随后,打开其他通道,并使用其他的注射泵调节通道内的灌注。
(作者:陈有灵犀 科学网科学网转载仅供参考学习及传递有用信息,版权归原作者所有,如侵犯权益,请联系删除)


